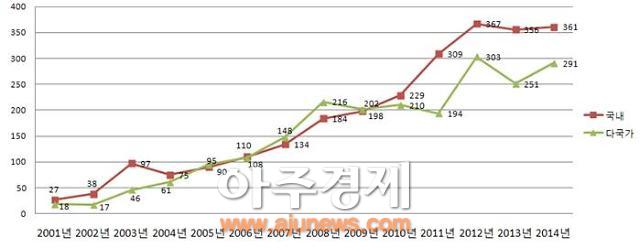
최근 10년간(2001~2014) 임상시험 승인 현황[자료=식품의약품안전처]
30일 식품의약품안전처가 2014년 임상시험계획 승인현황을 분석한 결과에 의하면 전체 승인건수는 652건으로 나타났다. 이는 2013년의 607건과 비교해 7.4% 증가한 수치다.
임상시험 승인현황도 매년 늘어 2010년 439건에서 503건(2011년), 670건(2012년), 607건(2013년), 652건(2014년)이었다.
국내 제약사 승인은 27건(2013년)에서 220건(2014년)으로 3% 감소했지만 같은기간 다국적 제약사는 248건에서 285건으로 15% 증가했다.
국내 제약사의 1상 임상시험(152건)은 2013년(130건) 대비 17% 증가했다. 최근 국내 제약사들이 복합제 등 개량신약 개발에 성공하면서 임상시험 등 연구·개발(R&D) 비용을 확대한 데 따른 것으로 분석된다.
실제로 복합제에 대한 임상시험은 2013년 63건에서 2014년 86건으로 36%나 증가했다. 다국적 제약사도 1상 임상시험이 2013년 25건에서 2014년 40건으로 60% 이상 상승했다.
효능군으로는 종양, 제제별로는 합성의약품에 집중됐다.
임상시험용 의약품을 효능군 별로 살펴보면 종양(210건), 심혈관계(89건), 중추신경계(58건), 내분비계(55건) 등의 순으로 많았다.
제제별로는 합성의약품이 465건(71%), 바이오의약품 169건(26%), 생약(한약)제제 18건(3%)으로 나타났다.
바이오의약품의 경우 유전자재조합의약품(109건), 세포·유전자치료제(31건), 생물학적제제(29건) 순으로 많았고, 유전자재조합의약품은 2013년(88건) 대비 24% 증가했다.
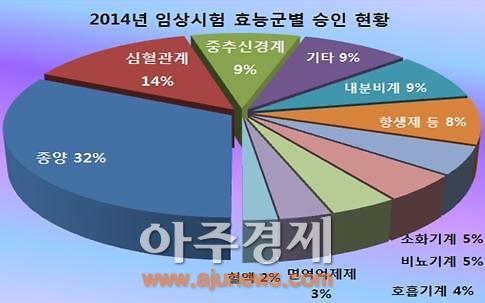
[자료=식품의약품안전처]
국내 제약사와 다국적 제약사간 효능별 임상분야는 서로 달랐다.
국내 제약사의 임상시험 건수는 심혈관계(60건), 내분비계(30건), 종양(20건), 비뇨기계(20건), 중추신경계(17건) 등의 순이었지만 다국적 제약사의 경우 종양(132건), 항생제(25건), 중추신경계(23건), 심혈관계(20건), 내분비계(20건) 등의 순서로 대조를 보였다.
특히, 항암제 임상시험은 2013년(101건) 대비 30% 이상 증가해 다국적 제약사들이 항암제 개발에 주력하고 있는 것으로 나타났다.
연구개발 수탁전문기업(CRO)의 임상시험 승인은 국내 제약사는 한미약품이 18건으로 가장 많았고, 일동제약(16건), 종근당(12건) 등이 뒤를 이었다.
다국적 제약사의 경우 한국노바티스(26건), 한국엠에스디(18건), 글락소스미스클라인(15건), 한국화이자(14건), 한국베링거인겔하임(13건), 한국아스트라제네카(13건) 등의 순이었다.
연구개발 수탁전문기업(CRO)은 퀸타일즈 트랜스내셔널코리아(31건), 피피디 디벨럽먼트피티이엘티디(15건), 파마수티컬리서치어소시에이츠코리아(15건) 순으로 많았다.
지역별 임상시험실시기관 별로는 서울(1518건, 53%)과 경기도(466건, 16%)가 약 70%를 차지 수도권에 편중됐다. 기타 지역은 부산(181건, 6%), 대구(157건, 5%), 인천(132건, 4%) 등의 순이었다.
지역별 편차는 수도권에 대형 임상시험실시기관이 많이 위치해 있기 때문으로 해석된다.
임상시험실시기관은 서울대학교병원(240건, 8.4%), 삼성서울병원(214건, 7.5%), 서울아산병원(194건, 6.8%), 연세대학교 신촌세브란스병원(192건, 6.7%), 가톨릭대학교 서울성모병원(136건, 4.7%) 등의 순서였고 이들 5개 대형 병원의 점유율은 34%로 나타나, 소위 '빅 5병원'이 앞도적이었다.
식약처는 국내 제약사 등이 체계적이고 효율적인 임상시험을 통해 신약을 개발 할 수 있도록 지속적인 지원을 수행하는 동시에 국제조화 및 품질향상은 물론 임상시험 참여자 안전을 강화할 계획이다.
©'5개국어 글로벌 경제신문' 아주경제. 무단전재·재배포 금지


![[르포] 중력 6배에 짓눌려 기절 직전…전투기 조종사 비행환경 적응훈련(영상)](https://image.ajunews.com/content/image/2024/02/29/20240229181518601151_258_161.jpg)



